L’ homme a toujours poursuivi le rêve d’atteindre l’immortalité et de franchir les limites de la vie. Mais qu’est-ce que d’un point de vue biologique ? L’espèce humaine pourrait-elle conquérir la mort un jour ? DGS vous apporte quelques éléments de réaction.
La quête d’immortalité n’a rien d’une vue de l’esprit. Sur Terre, ce concept se pare pourtant d’un nom plus précis : celui d’« immortalité biologique ». Comme le souligne Thomas Bosch, de l’université de Kiel en Allemagne : « Immortel signifie que vous ne mourrez pas du tout, ce qui est absurde. » En réalité, même les créatures dites « immortelles » restent vulnérables : proie des prédateurs, victimes de maladies ou de bouleversements environnementaux, aucun être vivant n’échappe totalement à la faucheuse si les circonstances s’en mêlent.
Lire également : Où trouver des témoignages de personnes qui ont vaincu l'agoraphobie ?

CERTAINS ORGANISMES NE SUBISSENT PAS LE TEMPS COMME LES AUTRES
A lire aussi : Tableau maladie professionnelle 57 délai de prise en charge : ce que votre employeur ne vous dit jamais
Certes, nul organisme n’est infaillible, mais certains défient tout de même les lois du vieillissement. Prenez le pin Bristlecone : ce conifère américain a vu le jour il y a près de 5000 ans pour les plus anciens spécimens. Howard Thomas, de l’université d’Aberystwyth au Royaume-Uni, s’enthousiasme : « Ces arbres sont incroyables. Ils affrontent la foudre, les tempêtes de neige, mais si l’on s’attarde sur leur fonctionnement interne, c’est une autre histoire. »
Une étude de 2001 a analysé le pollen et les tissus de pins Bristlecone âgés de 4700 ans et plus. Résultat : aucune augmentation du taux de mutation avec l’âge, et un système vasculaire aussi performant chez les anciens que chez les jeunes arbres. À l’œil nu, les branches des vétérans semblent fatiguées, mais au niveau cellulaire, rien n’a vraiment changé.

Le secret du pin Bristlecone ? Les chercheurs l’ignorent en grande partie, mais Howard Thomas avance une piste : tout se jouerait dans les « méristèmes », ces zones de croissance peuplées de cellules souches. Tant que ces cellules restent actives et indemnes de mutations majeures, l’arbre renouvelle sans cesse ses tissus. Si une cellule se détraque, d’autres prennent le relais, et la longévité continue.

Lieven De Veylder, de l’université de Gand en Belgique, propose une explication complémentaire. Dans les méristèmes, un « centre de repos » héberge des cellules qui se divisent très lentement, limitant ainsi l’accumulation de mutations. Selon De Veylder, « une sous-population de cellules souches à division rare permettrait de préserver un génome pratiquement intact ».
En 2013, l’équipe de De Veylder a identifié une protéine qui régule ce centre de repos chez la plante Arabidopsis. Il est probable que des protéines du même type aident aussi le pin Bristlecone à échapper au vieillissement cellulaire et à traverser les siècles. Toutefois, ce processus n’est pas infaillible : parfois, les méristèmes s’épuisent et entraînent la plante dans une sénescence accélérée, la condamnant à une vie brève.

QUAND DES PROTÉINES FREINENT L’USURE DU TEMPS
La découverte de la protéine impliquée dans la longévité d’Arabidopsis ouvre des perspectives fascinantes. Chez les plantes, la rapidité de division cellulaire peut jouer contre elles : Arabidopsis épuise ses organes avant que les méristèmes n’aient le temps de les renouveler. À l’inverse, les espèces à croissance lente, comme le pin Bristlecone, misent sur une activité méristématique réduite pour maximiser la durée de vie de chaque organe.

Chez les animaux, la règle générale veut que la vie soit plus courte que chez les plantes. Mais il existe des exceptions qui bousculent tout : les coraux, par exemple, vivent parfois plus de 4000 ans. Autre cas frappant : le quahog nordique, un coquillage découvert en Islande en 2006, dont l’analyse a révélé un âge de 507 ans. Ce spécimen, baptisé Ming, détient le record de longévité solitaire… ironie du sort, son âge fut déterminé au prix de sa mort.

Les membranes cellulaires de Ming présentaient une résistance exceptionnelle aux agressions oxydatives, d’après une étude de 2012. Les cellules de ce mollusque, tout comme celles du pin Bristlecone, accumulent les marques du temps à un rythme infiniment lent. Sans intervention extérieure, Ming aurait sans doute pu continuer sa vie séculaire.
En général, plus l’animal est petit, plus sa vie est brève. Pourtant, l’hydre échappe à la règle. Ce minuscule animal d’eau douce, proche parent des méduses, intrigue les biologistes. Maintenue en laboratoire pendant plus de quatre ans, l’hydre ne montrait aucun signe de vieillissement. À la fin de l’expérience, elle semblait aussi fraîche qu’au premier jour, un cas d’immortalité biologique individuelle qui force le respect.

Thomas Bosch et ses collègues ont percé une partie du mystère. L’hydre possède une réserve impressionnante de cellules souches capables de se transformer en n’importe quel tissu et de régénérer la moindre blessure. C’est cette faculté qui lui a valu son nom, inspiré de la créature mythologique capable de repousser ses têtes. L’hydre est, littéralement, une championne de la régénération.
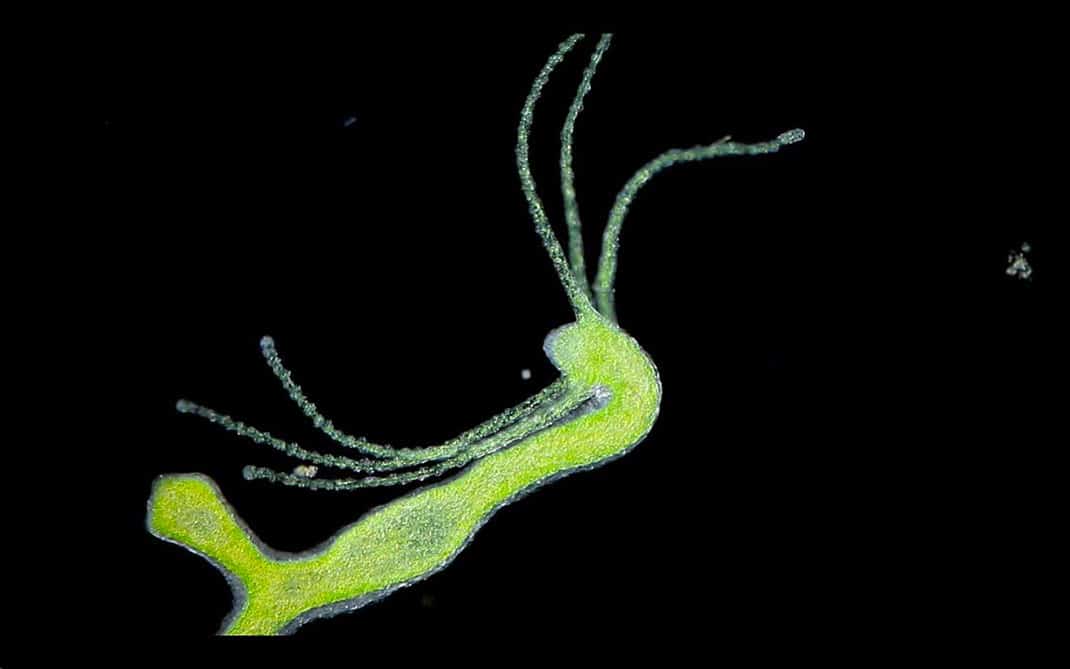
Cette capacité de renouvellement se retrouve dans sa façon de se reproduire : l’hydre ne passe pas par la reproduction sexuée, mais génère de petits clones d’elle-même. Trois types de cellules souches participent à la fabrication de tous les tissus nécessaires à un nouvel individu. Bosch et son équipe ont identifié un point commun à ces cellules : la présence d’une protéine appelée FoxO, soupçonnée de jouer un rôle majeur dans la lutte contre le vieillissement.
FOXO : UNE ARME ANTI-ÂGE PARTAGÉE PAR LE MONDE VIVANT ?
Le fonctionnement précis de FoxO reste à élucider. On sait déjà que cette protéine agit comme un chef d’orchestre, intégrant divers signaux internes et externes pour préserver la jeunesse cellulaire. Bosch poursuit actuellement ses recherches afin de comprendre comment l’environnement module l’action de FoxO. Plus fascinant encore : cette protéine n’est pas l’apanage de l’hydre. On en retrouve des variantes chez l’humain, notamment chez les centenaires, ce qui laisse entrevoir un mécanisme universel de longévité.

La méduse Turritopsis dohrnii pousse l’étrangeté un cran plus loin. Chez la plupart des méduses, la rencontre entre un spermatozoïde et un ovule donne une larve qui se fixe sur une surface, puis forme un polype. Ces polypes produisent généralement des clones d’eux-mêmes, mais, chez certaines espèces, ils génèrent aussi des méduses adultes. Ce cycle est déjà complexe, mais Turritopsis dohrnii défie les règles : même à l’état adulte et sexuellement mature, elle peut régresser et redevenir un polype, échappant ainsi à la mort biologique.
RETOUR EN ARRIÈRE : LA MÉDUSE QUI REFUSE DE MOURIR
Chez la majorité des méduses, cette faculté de rajeunissement s’arrête à la maturité sexuelle. Mais chez Turritopsis nutricula et Turritopsis dohrnii, le retour en arrière reste possible à tout moment. L’adulte peut redevenir polype, repartant pour un nouveau cycle de vie. Le mécanisme précis de ce rajeunissement reste à découvrir, mais il semble que la méduse inverse le processus cellulaire de son développement.
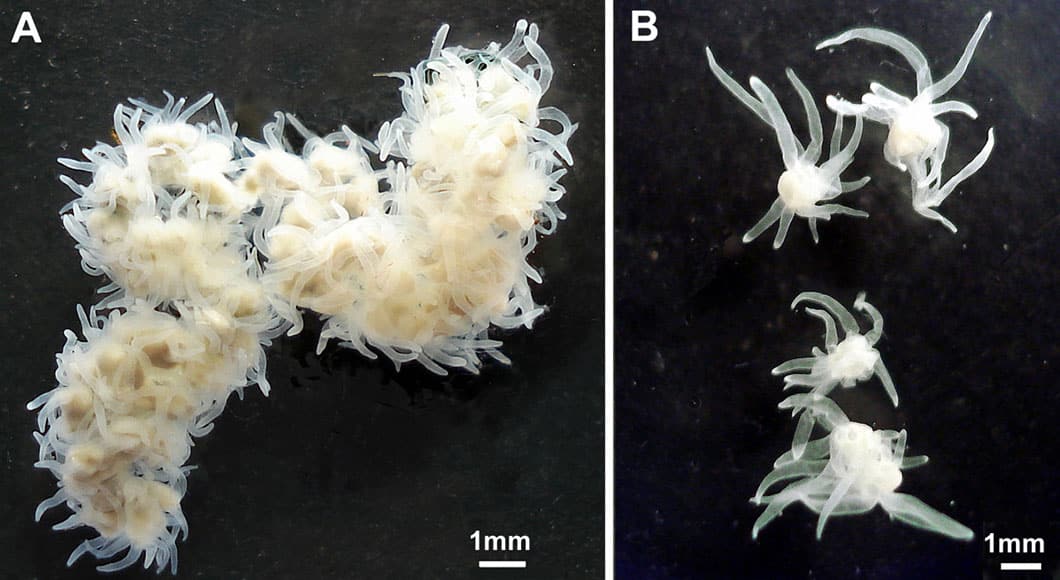
La reproduction asexuée et la capacité de rajeunir sont deux traits distinctifs des méduses, et ils pourraient bien être liés. D’après Thomas Bosch, les espèces capables de se cloner grâce à des cellules souches puissantes affichent cette « immortalité » cellulaire. À l’inverse, une reproduction essentiellement sexuée condamne presque toujours à une fin programmée.

Bosch avance une explication simple : la production de gamètes, ovules et spermatozoïdes, exige beaucoup d’énergie et finit par conduire l’animal à sa perte. Pourtant, même chez des animaux à reproduction sexuée, l’immortalité biologique n’est pas totalement hors de portée. Le homard américain en offre un exemple saisissant. Contrairement à la plupart des animaux, Homarus americanus continue de croître toute sa vie et peut même régénérer ses membres. Ces capacités de régénération restent intactes à un âge avancé, si bien que certains gros spécimens pourraient avoir plus de 140 ans.

LE SECRET DU HOMARD : DES CELLULES QUI PERDENT PEU DE LEUR JEUNESSE
La longévité du homard pourrait s’expliquer par la gestion très particulière de son ADN. Les chromosomes sont protégés à leurs extrémités par des télomères, qui raccourcissent à chaque division cellulaire. Chez la plupart des animaux, cette érosion amorce le vieillissement ; mais chez le homard, une enzyme, la télomérase, rallonge en permanence les télomères. Une étude de 1998 a montré que cette enzyme reste active dans tous les organes du crustacé, ce qui permet à ses cellules de conserver leur jeunesse et leur capacité à se diviser.
Cette astuce naturelle n’est pas unique au homard. On la retrouve aussi chez certains mammifères, dont l’humain, mais de façon bien plus restreinte.

Un cas célèbre illustre la puissance de ce mécanisme : celui d’Henrietta Lacks, décédée en 1951. Après sa mort, les scientifiques ont isolé de ses tumeurs utérines une lignée de cellules, les cellules HeLa, capables de se multiplier indéfiniment grâce à une activité forte de la télomérase. Ces cellules immortelles ont permis d’innombrables découvertes scientifiques, mais leur prolifération a coûté la vie à leur donneuse. Le paradoxe est total : l’immortalité cellulaire peut être à double tranchant.
Les cellules cancéreuses ne sont d’ailleurs pas les seules à échapper au vieillissement. Les cellules germinales humaines, responsables de la production des ovules et spermatozoïdes, sont également capables de préserver leur jeunesse. C’est ce qui explique que les enfants naissent « jeunes » à chaque génération, même si le phénomène mérite d’être précisé. Un exemple marquant : le cas du mouton Dolly, le premier mammifère cloné à partir de cellules adultes.
LES CELLULES GERMINALES : UNE JEUNESSE QUI SE TRANSMET
Dolly a vu le jour à partir de cellules mammaires d’un mouton adulte, qui portaient déjà les marques du temps. Le résultat : l’animal est né avec des télomères raccourcis et a vieilli prématurément, mourant d’une maladie pulmonaire à six ans, bien avant ses congénères non clonés.
Chez l’humain, la question de l’immortalité se résume à une interrogation : comment réinitialiser l’horloge cellulaire ? Howard Thomas l’affirme : tout repose sur la capacité à « remettre les compteurs à zéro ». Malgré les progrès de la recherche sur la télomérase, nous sommes encore loin de pouvoir inverser notre propre vieillissement.

Ce que révèlent toutes ces observations sur les espèces animales et végétales, c’est la diversité des stratégies mises en place pour repousser la limite du temps. À chaque découverte, la frontière entre vieillesse et jeunesse s’effrite un peu plus. Reste à savoir ce que l’avenir nous réserve : la cryogénisation, par exemple, continue d’alimenter l’espoir de suspendre la mort, pour mieux la défier un jour. Qui sait si, quelque part, une nouvelle énigme du vivant n’attend pas de bouleverser notre rapport au temps ?






